Logo and Menu
조선일보

국내 연구진이 알츠하이머병의 원인으로 알려진 아밀로이드베타 단백질이 만들어지는 원리를 찾았다. 아밀로이드베타가 만들어지는 양을 조절하면 알츠하이머병 예방과 치료에 활용할 수 있을 것으로 기대된다.
기초과학연구원(IBS)은 천진우 나노의학 연구단 단장이 이끄는 국제 공동 연구진이 지난달 2일 국제 학술지 ‘네이처 셀 바이올로지’에 “여러 세포가 연결될 때 만들어지는 구조가 세포 신호를 조절하는 데 중요한 역할을 하고, 이를 알츠하이머병의 치료제 개발에 활용할 수 있다”는 연구 결과를 발표했다고 10일 밝혔다.
알츠하이머병은 뇌에 비정상적인 아밀로이드베타 단백질이 쌓이면서 세포의 기능과 기억, 언어, 행동 능력이 떨어지는 질병이다. 아밀로이드베타는 신경세포에서 만들어지는 기본 형태인 전구체 단백질이 차례대로 두 번 잘리면서 만들어지는 데, 전구체가 잘리면서 아밀로이드베타가 되는 과정을 찾아서 아밀로이드베타가 만들어지는 것을 막을 수 있다면 알츠하이머병을 예방하거나 치료할 수 있다.
IBS 연구진은 아밀로이드베타의 생성을 조절하는 방법을 찾기 위해 ‘노치 신호전달’에 주목했다. 노치 신호전달은 신경 세포의 발달을 조절하고, 아밀로이드베타와 마찬가지로 전구체인 노치 수용체가 잘리면서 활성화된다. 또 아밀로이드베타 전구체와 노치 수용체는 모두 세포 막에 있는 효소에 의해 잘리는 것으로 알려졌다. 노치 신호전달에 필요한 절단 과정을 밝혀서 아밀로이드베타의 생성을 조절하는 방법을 찾는다는 전략이다.
IBS 연구진은 유전자 가위로 세포의 접착에 중요한 역할을 하는 카드헤린 단백질이 만들어지지 않도록 쥐의 유전자를 편집했다. 카드헤린 단백질이 만들어지지 않는 쥐는 세포의 접착이 제대로 일어나지 않으면서 노치 신호가 활성화되지 않았다. 또 발달 중인 뇌의 신경줄기세포에서 카드헤린 발현을 줄이자, 줄기세포는 비정상적으로 빠르게 신경세포로 변했다. 세포의 접착이 노치 신호에 영향을 주고 신경계 발달에도 중요한 역할을 한다는 결과다.
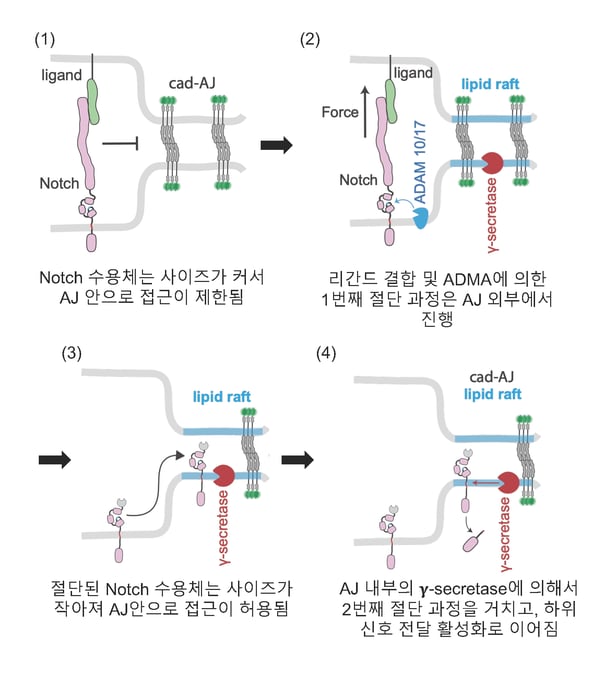
IBS 연구진은 세포의 접착 구조가 노치 신호전달에 영향을 미치는 이유를 단백질의 크기 때문으로 분석했다. 세포의 접착 구조에 있는 절단 효소인 ADAM이 노치 수용체를 잘라 크기를 작게 만들고, 작아진 노치 수용체가 좁은 공간에 들어가야 제대로 기능을 할 수 있다는 것이다.
실제로 아밀로이드베타 단백질의 양도 세포의 접착 구조에 따라서 달라졌다. 아밀로이드베타의 전구체를 만드는 세포의 접착을 막자, 전구체가 잘리지 않으면서 아밀로이드베타가 만들어지는 양이 줄었다. IBS 연구진은 세포의 접착 구조가 단백질의 절단에 중요한 역할을 하는 만큼, 세포의 접착 구조를 통해 단백질의 절단을 막으면 아밀로이드베타가 만들어지는 양을 조절할 수 있을 것으로 전망했다.
곽민석 IBS 나노의학 연구단 연구위원은 “이번 연구를 통해 비정상적인 아밀로이드베타 때문에 나타나는 알츠하이머병의 치료제 개발에 기여할 수 있을 것으로 기대한다”며 “노치 신호를 조절해 신경계 발달 과정을 모사하는 뇌 유사체 개발로도 연구를 확장할 것”이라고 말했다.
Copyright and Address
- Yonsei Advanced Science Institute
- PRIVACY POLICY



- ADDRESS IBS Hall 50 Yonsei-ro, Seodaemun-gu, Seoul 03722
- TEL +82-2-2123-4769 FAX +82-2-2123-4606
- E-MAIL ibs@yonsei.ac.kr
- Copyright © IBS Center for NanoMedicine,YONSEI UNIV.
ALL RIGHTS RESERVED.

